Yksi maailma yksi taistelu
─ Kansainvälinen yhteistyö COVID-19-pandemian haasteen globaalin yhteisen kohtalon yhteisön rakentamiseksi
Romaani Coronavirus-lakaisu ympäri maailmaa on johtanut meneillään olevaan globaaliin COVID-19-pandemiakriisiin. Coronavirus-romaanissa ei ole rajoja, mikään maa ei säästetä tästä taistelusta Covid-19: tä vastaan. Vastauksena tähän maailmanlaajuiseen COVID-19-pandemiaan, Liming Bio -tuotteet Corp antaa panoksia globaalien yhteisöidemme hyvinvoinnin tukemiseen.
Maailmamme on tällä hetkellä kohtaavat uuden Coronavirus-taudin 2019 (COVID-19) pandemian ennennäkemättömän vaikutuksen. Tähän päivään mennessä tämän taudin hoitoon ei ole käytettävissä tehokasta lääkettä. COVID-19: n havaitsemiseksi on kuitenkin kehitetty monia diagnostisia testejä. Nämä testit perustuvat molekyyli- tai serologisiin menetelmiin uusien koronavirusspesifisten nukleiinihappo- tai vasta -ainebiomarkkereiden havaitsemiseksi. Koska COVID-19 on saavuttanut pandemisen tilan, uuden koronavirusinfektion varhainen diagnoosi on kriittistä viruksen leviämisen ja sen sisältämisen arvioinnissa, mutta täydellistä testiä yleiseen käyttöön ei vielä ole. Meidän on tiedettävä, mitä testejä voidaan mahdollisesti käyttää COVID-19-infektion seulontaan, diagnosointiin ja seurantaan ja mitkä ovat niiden rajoitukset. On erittäin tärkeää, kuinka käyttää paremmin näitä tieteellisiä työkaluja ja auttaa tunnistamaan ja hallitsemaan tämän nopeasti leviävän ja vakavan sairauden syntymistä.
Uuden koronaviruksen havaitsemisen tarkoituksena on selvittää, onko henkilö, jolla on COVID-19-infektio vai asymptoottinen kantaja, joka voi levittää virusta hiljaa, tarjota välttämätöntä tietoa päätöksenteon ohjaamiseksi kliiniseen hoitoon. Aikaisemmat tutkimukset ovat osoittaneet, että 70% kliinisistä päätöksistä riippuu testaustuloksista. Kun käytetään erilaisia havaitsemismenetelmiä, myös havaitsemisreagenssisarjojen vaatimukset ovat erilaisia.
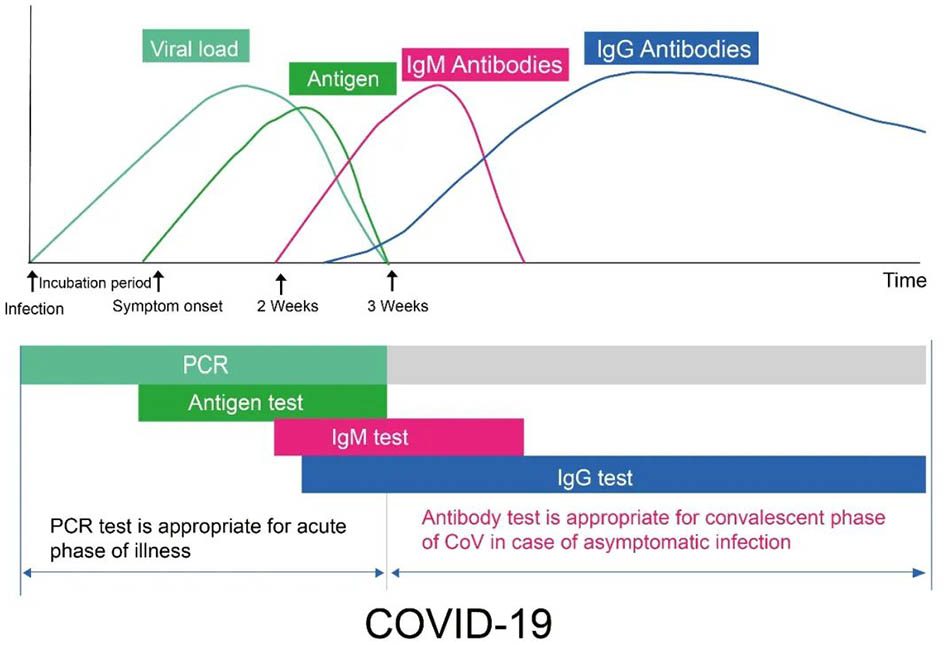
Kuva 1
Kuva 1:Kaavio, joka näyttää yleisten biomarkkeritasojen avainvaiheet COVID-19-infektion tyypillisellä kululla. X-akseli osoittaa infektiopäivien lukumäärän, ja y-akseli osoittaa viruskuorman, antigeenien pitoisuuden ja vasta-aineiden pitoisuuden eri ajanjaksoina. Vasta -aine tarkoittaa IgM- ja IgG -vasta -aineita. Sekä RT-PCR: n että antigeenin havaitsemista käytetään uuden koronaviruksen esiintymisen tai puuttumisen havaitsemiseksi, mikä on suora näyttö potilaiden varhaisesta havaitsemisesta. Viikon kuluessa virusinfektiosta, PCR: n havaitsemisesta tai antigeenin havaitsemisesta on edullista. Uuden koronavirusinfektion jälkeen noin 7 päivän ajan IgM -vasta -aine uutta koronavirusta vastaan on vähitellen lisääntynyt potilaan veressä, mutta olemassaolon kesto on lyhyt ja sen pitoisuus laskee nopeasti. Sitä vastoin IgG -vasta -aine virusta vastaan ilmestyy myöhemmin, yleensä noin 14 päivää virusinfektion jälkeen. IgG -pitoisuus kasvaa vähitellen, ja se jatkuu pitkään veressä. Siten, jos IgM havaitaan potilaan veressä, se tarkoittaa, että virus on äskettäin tartunnan saanut, mikä on varhainen infektiomerkki. Kun IgG -vasta -aine havaitaan potilaan veressä, se tarkoittaa, että virusinfektio on ollut jonkin aikaa. Sitä kutsutaan myös myöhäiseksi infektioksi tai aikaisemmaksi infektioksi. Se nähdään usein potilailla, jotka ovat palautumisvaiheessa.
Uuden koronaviruksen biomarkkerit
Uusi koronavirus on RNA -virus, joka koostuu proteiineista ja nukleiinihapoista. Virus tunkeutuu isäntä (ihmisen) kehoon, menee soluihin sitoutumiskohdan kautta, joka vastaa reseptoria ACE2 ja replikoituu isäntäsoluissa, aiheuttaen ihmisen immuunijärjestelmän reagoimaan vieraisiin hyökkääjiin ja tuottamaan spesifisiä vasta -aineita. Siksi injektiopullon nukleiinihappoja ja antigeenejä ja spesifisiä vasta -aineita uutta koronavirusta vastaan voidaan teoreettisesti käyttää spesifisinä biomarkkereina uuden koronaviruksen havaitsemiseksi. Nukleiinihapon havaitsemiseksi RT-PCR-tekniikka on yleisimmin käytetty, kun taas serologisia menetelmiä käytetään yleisesti uuden koronavirusspesifisten vasta-aineiden havaitsemiseen. Tällä hetkellä on saatavana erilaisia testimenetelmiä, jotka voimme valita COVID-19-infektion testaamiseksi [1].
Uuden koronaviruksen päätestien perusperiaatteet
Tähän mennessä on saatavana monia COVID_19 -diagnostisia testejä, ja enemmän testisarjoja saa hyväksynnän hätäkäytön luvan perusteella päivittäin. Vaikka uudet testikehitykset, jotka tulevat esiin niin monella eri nimellä ja muodolla, kaikki nykyiset COVID_19-testit luottavat periaatteessa kahteen pääteknologiaan: nukleiinihapon havaitseminen virus-RNA: lle ja serologisille immunomäärityksille, jotka havaitsevat virusspesifiset vasta-aineet (IGM ja IGG).
01. Nukleiinihapon havaitseminen
Käänteinen transkription polymeraasiketjureaktio (RT-PCR), silmukkavälitteinen isoterminen monistus (LAMP) ja seuraavan sukupolven sekvensointi (NGS) ovat yleisiä nukleiinihappomenetelmiä uuden koronavirus-RNA: n havaitsemiseksi. RT-PCR on COVID-19: n ensimmäinen testityyppi, jota suosittelee sekä Maailman terveysjärjestö (WHO) että Yhdysvaltain tautien torjunta- ja ehkäisykeskus (CDC).
02. Serologinen vasta -aineiden havaitseminen
Vasta -aine on ihmiskehossa tuotettu suojaproteiini vasteena virusinfektiolle. IgM on varhainen vasta -ainetyyppi, kun taas IgG on myöhempi tyyppinen vasta -aine. Seerumin tai plasmanäytettä tutkitaan yleensä vasta-aineen spesifisten IgM- ja IgG-tyyppien läsnäolon suhteen COVID-19-infektion akuutin ja toipustofaasien arvioimiseksi. Nämä vasta-ainepohjaiset havaitsemismenetelmät sisältävät kolloidisen kullan immunokromatografiamäärityksen, lateksi- tai fluoresoivan mikrofäärin immunokromatografian, entsyymisidosten immunosorbenttimäärityksen (ELISA) ja kemiluminesenssimäärityksen.
03.Viraalinen antigeenin havaitseminen
Antigeeni on ihmiskehon tunnistaman viruksen rakenne, joka laukaisee immuunipuolustusjärjestelmän tuottamaan vasta -aineita viruksen puhdistamiseksi verestä ja kudoksista. Viruksen läsnä oleva virusantigeeni voidaan kohdistaa ja havaita immunomäärityksellä. Virus-RNA: n tavoin virusantigeenejä esiintyy myös tartunnan saaneiden yksilöiden hengitysteissä, ja niitä voidaan käyttää COVID-19-infektion akuuttifaasin diagnosointiin. Siksi on usein suositeltavaa kerätä ylähengitysteenäytteitä, kuten sylkeä, nenänielun ja orofaryngeaalisia swabeja, syvän yskän ysköä, bronkoalveolaarista huuhtelunestettä (BALF) alkuperäistä antigeenitestausta varten.
Testausmenetelmien valitseminen uudelle koronavirukselle
Testausmenetelmän valitseminen sisältää monia tekijöitä, mukaan lukien kliininen asetus, laadunvalvonta, käännösaika, testauskustannukset, näytteenottomenetelmät, laboratorion henkilöstön tekniset vaatimukset, laitos- ja laitevaatimukset. Nukleiinihappojen tai virusantigeenien havaitseminen on tarjota suora näyttö virusten läsnäolosta ja vahvistaa uuden koronavirusinfektion diagnoosi. Vaikka antigeenien havaitsemiseksi on monia menetelmiä, niiden uuden koronaviruksen havaitsemisherkkyys on teoreettisesti alhaisempi kuin RT-PCR-monistuksen. Vasta-ainetestaus on ihmiskehossa tuotettujen virusviruksen vasta-aineiden havaitseminen, joka on ajan myötä viivästynyt ja jota ei usein voida käyttää varhaisessa havaitsemisessa virusinfektion akuutin vaiheen aikana. Tunnistussovellusten kliininen asetus voi vaihdella, ja myös näytteenkeruupaikat voivat olla erilaisia. Virusnukleiinihappojen ja antigeenien havaitsemiseksi näyte on kerättävä hengitysteissä, joissa virusta on läsnä, kuten nenänielun nielun, orofaryngeaalisten swabinit, ysköt tai bronkoalveolaariset huuhtoveden (BALF). Vasta-ainepohjaista havaitsemista varten verinäytteet on kerättävä ja tutkittava spesifisen virusvasta-aineen (IgM/IgG) läsnäolon suhteen. Vasta -aine- ja nukleiinihappokoetulokset voivat kuitenkin täydentää toisiaan. Esimerkiksi, kun testaustulos on nukleiinihappo-negatiivinen, IgM-negatiivinen, mutta IgG-positiivinen, nämä tulokset osoittavat, että potilaalla ei tällä hetkellä ole virusta, mutta on otettu talteen uudesta koronavirusinfektiosta. [2]
Uusien koronaviruskokeiden edut ja haitat
Uuden koronaviruksen keuhkokuumeen diagnoosi- ja hoitoprotokolla (tutkimusversio7) (perinteisen kiinalaisen lääketieteen kansallisen terveyskomission ja valtionhallinnon julkaisema 3. maaliskuuta 2020) nukleiinihappotestausta käytetään kultastandardimenetelmänä romaanin diagnoosissa Coronavirus -infektio, kun taas vasta -ainetestausta pidetään myös yhtenä diagnoosin vahvistusmenetelmistä.

Patogeeniset ja serologiset havainnot
(1) Patogeeniset löydökset: Uudet koronavirus-nukleiinihappot voidaan havaita nenänielun nielun, veren, ulosteiden ja muiden näytteiden alahengitysteiden erityksissä, veressä, ulosteessa ja muissa näytteissä käyttämällä RT-PCRAND/tai NGS-menetelmiä. On tarkempi, jos näytteet saadaan alahengitysteistä (yskö tai ilmateiden uuttaminen). Näytteet on toimitettava testattavaksi mahdollisimman pian keräämisen jälkeen.
(2) serologiset löydökset: NCP-viruskohtainen IGM tulee havaittavissa noin 3-5 päivää alkamisen jälkeen; IgG saavuttaa vähintään 4-kertaisen nousun titrauksen toipumisen aikana verrattuna akuuttiin vaiheeseen.
Testausmenetelmien valinta riippuu kuitenkin maantieteellisistä paikoista, lääketieteellisistä määräyksistä ja kliinisistä olosuhteista. Yhdysvalloissa NIH julkaisi Coronavirus-taudin 2019 (COVID-19) hoito-ohjeet (sivusto päivitetyt: 21. huhtikuuta 2010) ja FDA: n julkaistut politiikan CORONAVIRUS-taudin diagnostisten testien suorittamisesta 2019 kansanterveyden hätätilanteessa (annettu 16. maaliskuuta 201020 ), jossa IgM/IgG -vasta -aineiden serologinen testaus valittiin vain seulontakokeeksi.
Nukleiinihapon havaitsemismenetelmä
RT_PCR on erittäin herkkä nukleiinihappotesti, joka on suunniteltu havaitsemaan, onko uusi koronavirus -RNA hengitys- tai muussa näytteessä. Positiivinen PCR-testitulos tarkoittaa uuden koronavirus-RNA: n läsnäoloa näytteessä COVID-19-infektion vahvistamiseksi. Negatiivinen PCR -testitulos ei tarkoita virusinfektion puuttumista, koska siihen voi vaikuttaa siihen, että heihin voi vaikuttaa huono näytteen laatu tai sairausaika, jne. Vaikka RT-PCR on erittäin herkkä testi, sillä on useita haittoja. RT-PCR-testit voivat olla työvoimavaltaisia ja aikaa vieviä, ratkaisevia näytteen korkeasta laadusta. Tämä voi olla haaste, koska virus -RNA: n määrä ei vain vaihtele valtavasti eri potilaiden välillä, vaan voi myös vaihdella samassa potilaassa riippuen ajankohdista, kun näyte kerätään, samoin kuin infektiovaiheet tai kliinisten oireiden alkaminen. Uuden koronaviruksen havaitseminen vaatii korkealaatuisia näytteitä, jotka sisältävät riittävän määrän ehjää virus-RNA: ta.
RT-PCR-testi voi antaa väärän negatiivisen tuloksen (väärä negatiivinen) joillekin potilaille, joilla on COVID-19-infektio. Kuten tiedämme, uuden koronaviruksen tärkeimmät infektiokohdat sijaitsevat keuhkoissa ja alahengitysteissä, kuten alveolit ja keuhkoputket. Siksi syvän yskän tai bronkoalveolaarisen huuhtelunesteen (BALF) ysköinäytteillä, joiden katsotaan olevan suurin herkkyys viruksen havaitsemiseksi. Kliinisessä käytännössä näytteet kuitenkin kerätään usein ylähengitysteistä käyttämällä nenänielun tai orofaryngeaalisia taisteluita. Näiden näytteiden kerääminen ei ole vain epämiellyttävää potilaille, vaan vaatii myös erityisesti koulutettua henkilöstöä. Jotta näytteenotto on vähemmän invasiivinen tai helpompi, joissakin tapauksissa potilaille voidaan antaa suun kautta annettava taistelu ja antaa heille mahdollisuuden ottaa näytteen bukcal -limakalvosta tai kielestä itseään. Ilman riittävää virus-RNA: ta, RT-QPCR voi palauttaa väärän negatiivisen testituloksen. Hubein maakunnassa Kiinassa RT-PCR-herkkyys alkuperäisessä havaitsemisessa ilmoitettiin vain noin 30%-50%, keskimäärin 40%. Väärin negatiivisen korkean määrän aiheutti todennäköisimmin riittämättömän näytteenotto.
Lisäksi RT-PCR-testi vaatii korkeasti koulutettua henkilöstöä monimutkaisten RNA-uuttovaiheiden ja PCR-monistusmenettelyn suorittamiseksi. Se vaatii myös korkeamman bioturvallisuussuojan, erityisen laboratoriolaitoksen ja reaaliaikaisen PCR-instrumentin. Kiinassa RT-PCR-testi COVID-19-havaitsemiseksi on suoritettava bioturvallisuustason 2 laboratorioissa (BSL-2) henkilöstösuojauksella käyttämällä bioturvallisuustason 3 (BSL-3) käytäntöä. Näiden vaatimusten nojalla tammikuun alusta helmikuun alkuun 2020 Kiinan Wuhanin CDC -laboratorion kapasiteetti pystyi havaitsemaan vain muutama sata tapausta päivässä. Yleensä tämä ei olisi ongelma testattaessa muita tartuntatauteja. RT-PCR: stä tulee kuitenkin kriittinen kysymys erityisten laboratoriolaitosten tai teknisten laitteiden vaatimusten vuoksi, kun käsitellään maailmanlaajuista pandemiaa, kuten COVID-19, ja mahdollisesti miljoonat ihmiset testataan. Nämä haitat voivat rajoittaa RT-PCR: ää käytettäväksi tehokkaana työkaluna seulontaan, ja ne voivat myös johtaa testitulosten raporteissa viivästyksiin.
Serologinen vasta -aineiden havaitsemismenetelmä
Taudin etenemisen myötä, etenkin keski- ja myöhäisissä vaiheissa, vasta -aineiden havaitsemisnopeus on erittäin korkea. Wuhanin keskustassa sairaalassa tehdyn tutkimuksen osalta osoitti, että vasta-aineiden havaitsemisaste voi saavuttaa yli 90% COVID-19-infektion kolmannella viikolla. Vasta -aine on myös ihmisen immuunivasteen tuote uutta koronavirusta vastaan. Vasta-ainekoe tarjoaa useita etuja RT-PCR: ään verrattuna. Ensinnäkin serologiset vasta -ainekokeet yksinkertaiset ja nopeat. Vasta-ainetta sivuttaisvirtauskokeita voidaan käyttää hoitopisteeseen tuloksen tuottamiseksi 15 minuutissa. Toiseksi serologisella testillä havaittu kohde on vasta -aine, jonka tiedetään olevan paljon stabiilempi kuin virus -RNA. Keräyksen, kuljetuksen, varastoinnin ja testauksen aikana vasta-ainekokeiden näytteet ovat yleensä vakaampia kuin RT-PCR: n näytteet. Kolmanneksi, koska vasta -aine jakautuu tasaisesti verenkiertoon, näytteenottovariaatio on vähemmän verrattuna nukleiinihappotestiin. Vasta -ainekokeen vaadittava näytteen tilavuus on suhteellisen pieni. Esimerkiksi 10 mikrolitraa sormenpihasta verestä on riittävä käytettäväksi vasta-aineen sivuttaisvirtaustestissä.
Yleensä vasta -ainekoe valitaan nukleiinihappojen havaitsemiseen liittyväksi työkaluksi uuden koronaviruksen havaitsemisnopeuden parantamiseksi taudikurssien aikana. Kun vasta-ainetestiä käytetään yhdessä nukleiinihappokokeen kanssa, se voi lisätä määritystarkkuutta COVID19: n diagnoosissa vähentämällä mahdollisia vääriä positiivisia ja vääriä negatiivisia tuloksia. Nykyinen operaatio -opas ei suosittele kahden tyyppisen testin käyttämistä erikseen riippumattomana havaitsemismuotona, mutta sitä tulisi käyttää yhdistelmämuotona. [2]
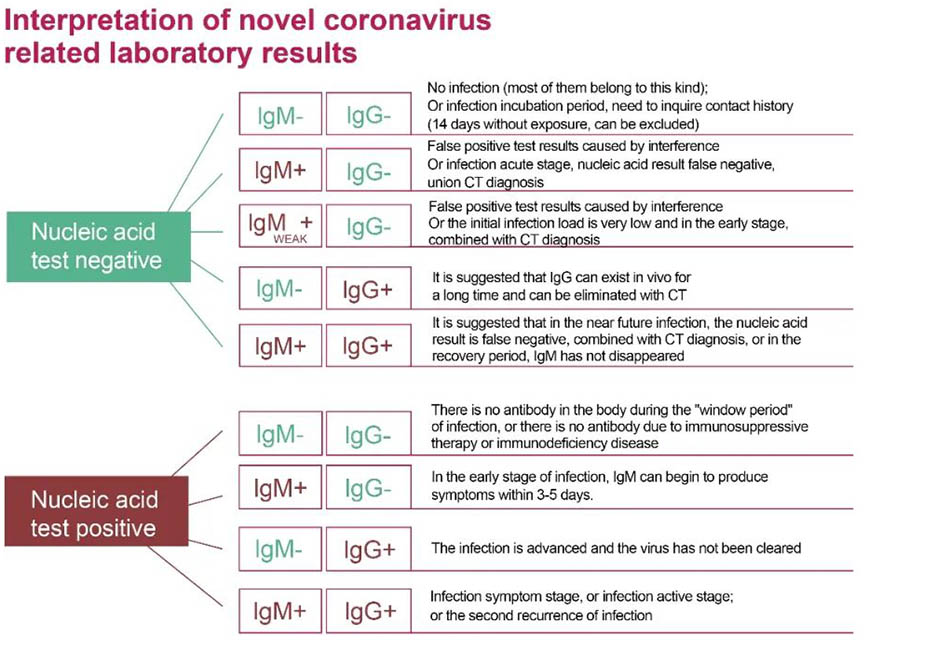
Kuva 2:Nukleiinihappo- ja vasta -ainekoetulosten oikea tulkinta uuden koronavirusinfektion havaitsemiseksi

Kuva 3:Liming Bio-Products Co., Ltd.-Uusi koronavirus IgM/IgG-vasta-aine kaksoispohjainen testipakkaus (StrongStep®SARS-COV-2 IgM/IgG-vasta-aine Rapid Test, lateksi-immunokromatografia))

Kuva 4:Liming Bio-Products Co., Ltd.-Vahvuusvaihe®Uusi koronavirus (SARS-COV-2) multipleksinen reaaliaikainen PCR-pakkaus (havaitseminen kolmelle geenille, fluoresoiva koetinmenetelmä).
Huomaa:Tämä erittäin herkkä, käyttövalmis PCR-pakkaus on saatavana lyofilisoidussa muodossa (pakastekuivausprosessi) pitkäaikaista varastointia varten. Pakkaus voidaan kuljettaa ja varastoida huoneenlämpötilassa ja on vakaa yhden vuoden ajan. Each tube of premix contains all of the reagents needed for the PCR amplification, including Reverse-transcriptase, Taq polymerase, primers, probes, and dNTPs substrates.Users can simply reconstitute the mix by adding PCR-grade water along with the template and then load PCR -instrumentin päälle vahvistuksen suorittamiseksi.
Vastauksena Coronavirus-puhkeamiseen, Liming Bio Products Co., Ltd. on työskennellyt nopeasti kehittääkseen kaksi diagnostisia sarjoja, jotta kliiniset ja kansanterveyslaboratoriot voidaan diagnosoida nopeasti COVID-19-tartunnan. Nämä sarjat ovat erittäin sopivia käytettäväksi laajamittaiseen seulontaan maissa ja alueilla, joilla uusi koronaviruksen puhkeaminen on nopeasti leviämässä, ja diagnoosin ja vahvistuksen tarjoamiseen COVID-19-tartuntaan. Nämä sarjat on käytettävä vain ennalta ilmoitetussa hätäkäytön valtuutuksessa (PEUA). Testaus on rajoitettu laboratorioihin, jotka on sertifioitu kansallisten tai paikallisten viranomaisten asetusten nojalla.
Antigeenin havaitsemismenetelmä
1. Virusantigeenin havaitseminen luokitellaan samaan suoran havaitsemisen luokkaan kuin nukleiinihapon havaitseminen. Nämä suorat havaitsemismenetelmät etsivät todisteita näytteen viruspatogeeneistä ja niitä voidaan käyttää vahvistusdiagnoosiin. Antigeenin havaitsemispakettien kehitys vaatii kuitenkin monoklonaalisten vasta -aineiden korkeaa laatua voimakkaan affiniteetin ja korkean herkkyyden, jotka kykenevät tunnistamaan ja vangitsemaan patogeenisiä viruksia. Monoklonaalisen vasta -aineen valitseminen ja optimointi vie yleensä yli kuusi kuukautta, jotka sopivat käytettäväksi antigeenin havaitsemispakkauksen valmistuksessa.
2. Tällä hetkellä uuden koronaviruksen suoran havaitsemisen reagenssit ovat edelleen tutkimus- ja kehitysvaiheessa. Siksi mitään antigeenin havaitsemispakkausta ei ole kliinisesti validoitu ja kaupallisesti saatavana. Vaikka aikaisemmin ilmoitettiin, että Shenzhenin diagnostiikkayritys on kehittänyt antigeenin havaitsemispakkauksen ja testattu kliinisesti Espanjassa, määrityksen luotettavuutta ja tarkkuutta ei voitu validoida reagenssin laatuongelmien läsnäolon vuoksi. Tähän päivään mennessä NMPA (entinen China FDA) ei ole vielä hyväksynyt mitään antigeenin havaitsemisarjaa kliiniseen käyttöön. Yhteenvetona voidaan todeta, että on kehitetty erilaisia havaitsemismenetelmiä. Jokaisella menetelmällä on etuja ja rajoituksiaan. Eri menetelmien tuloksia voidaan käyttää todentamiseen ja täydentämiseen.
3. Laadun COVID-19-testisarjan tuottaminen riippuu voimakkaasti optimoinnista tutkimuksen ja kehityksen aikana. Liming Bio-Product Co., Ltd. Testisarjoja vaaditaan täyttämään tiukat valmistus- ja laadunvalvontastandardit sen varmistamiseksi, että ne tarjoavat korkeimman suorituskyvyn ja johdonmukaisuuden. Liming Bio-Product Co., Ltd. -yrityksen tutkijoilla on yli kaksikymmentä vuoden kokemus in vitro -diagnostisten sarjojen suunnittelusta, testaamisesta ja optimoinnista korkeimman suorituskyvyn varmistamiseksi analyyttisessä kvantifioinnissa.
COVID-19-pandemian aikana Kiinan hallitus kohtasi valtavan kysynnän epidemian ehkäisymateriaaleista kansainvälisissä hotspotissa. Valtioneuvoston yhteisen ennaltaehkäisyn ja valvontamekanismin lehdistötilaisuudessa 5. huhtikuuta "lääketieteellisten materiaalien laadunhallinnan vahvistaminen ja markkinoiden järjestyksen säänteleminen", Jiang Fan, ministeriön ulkomaankaupan osaston ensimmäisen tason tarkastaja Commerce, sanoi: "Seuraavaksi keskitymme pyrkimyksemme kahteen näkökohtaan ensin nopeuttaaksemme kansainvälisen yhteisön tarvittavien lääketieteellisten tarvikkeiden tukea ja myös tuotteiden laadunvalvonnan, sääntelyn ja hallinnan parantamiseksi. Annamme Kiinan panoksen reagoimaan yhdessä globaaliin epidemiaan ja rakentamaan yhteisöä ja yhteistä tulevaisuutta ihmiskunnalle.



Kuva 5:Liming Bio Products Co., Ltd .: n uusi Coronavirus-reagenssi on saanut EU: n rekisteröintitodistuksen
Kunniatodistus


Houshenshan
Kuva 6. Liming Bio Products Co., Ltd. tuki Wuhan Vulcan (Houshenshan) vuoristosairaalaa taistelemaan COVID-19-epidemiaa vastaan ja sai Wuhan Punaisen Ristin kunniatodistuksen. Wuhan Vulcan Mountain Hospital on Kiinan tunnetuin sairaala, joka on erikoistunut vaikean covidin - 19 potilaan hoitoon.
Kun romaani Coronavirus-puhkeaminen jatkaa leviämistä ympäri maailmaa, Nanjing Liming Bio Products Co., Ltd. on tukemassa ja auttamassa yhteisöjä maailmanlaajuisesti innovatiivisten tekniikoidemme kanssa tämän ennennäkemättömän globaalin uhan torjumiseksi. COVID-19-infektion nopea testaus on kriittinen osa tämän uhan torjumista. Jatkamme merkittävästi lisäämällä korkealaatuisia diagnostiikkaalustoja etulinjan terveydenhuollon työntekijöiden käsiin, jotta ihmiset voivat saada tarvitsemansa kriittiset testaustulokset. Liming Bio Products Co., Ltd .: n pyrkimykset taistelussa COVID-19-pandemian torjunnassa on edistää tekniikoitamme, kokemuksiamme ja asiantuntemusta kansainvälisille yhteisöille globaalin kohtaloyhteisön rakentamiseksi.
Pitkä paina ~ Skannaa ja seuraa meitä
Sähköposti: sales@limingbio.com
Verkkosivusto: https://limingbio.com
Viestin aika: toukokuu-01-2020







