Vahvajärjestelmän laite SARS-COV-2 Antigeenin nopeaan testiin
Tarkoitettu käyttö
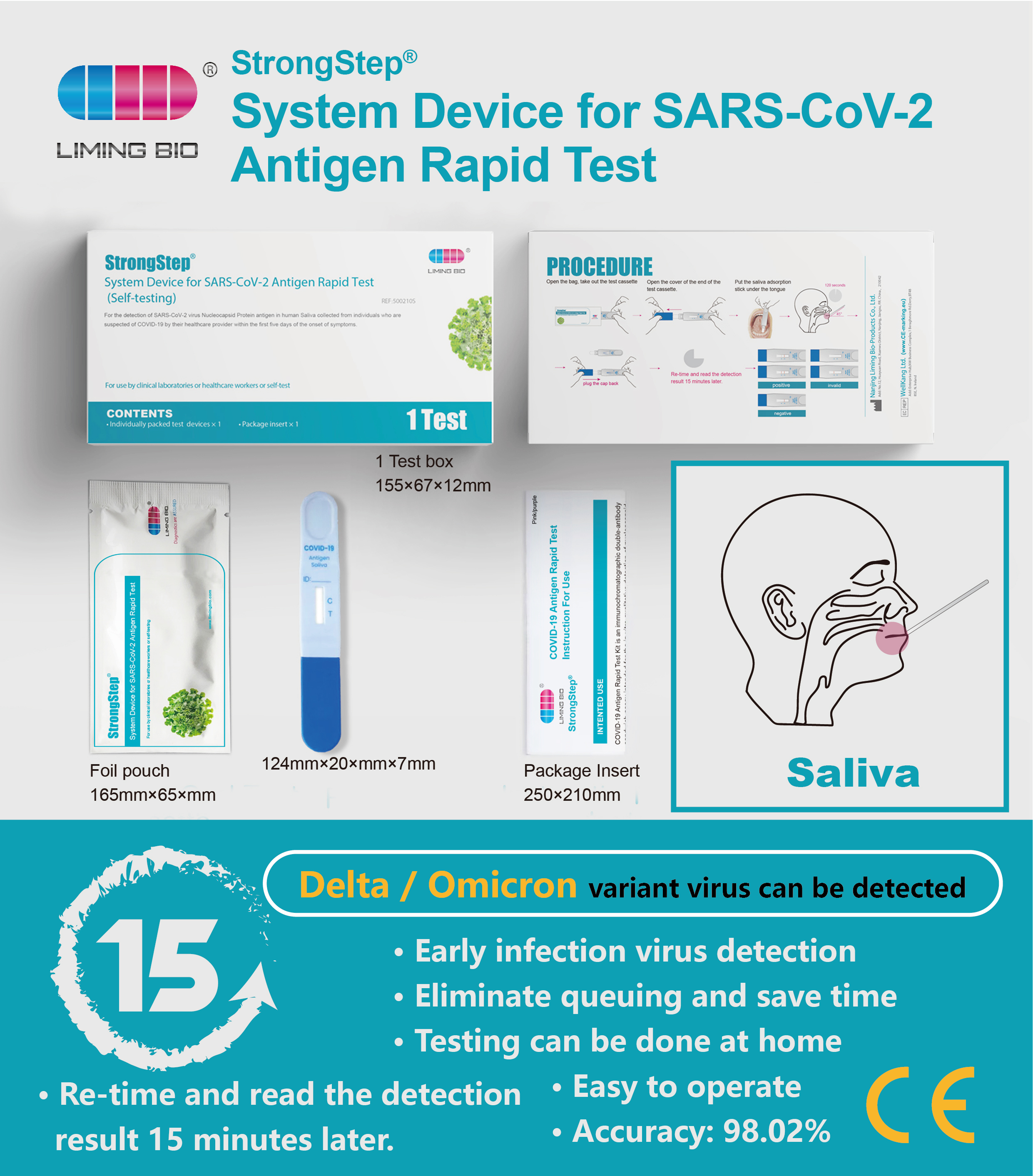
StrongStep®-järjestelmän laite SARS-COV-2-antigeenin nopeaan testiin käyttää immunokromatografiatekniikkaa SARS-COV-2-nukleokapsidigeenin havaitsemiseksi ihmisen sylissä. Tämä testi on vain yksi käyttö ja tarkoitettu SEI: lle - testi. Tätä testiä suositellaan käyttämään 7 päivän kuluessa oireiden alkamisesta, sitä tukee kliininen suorituskyvyn arviointi.
Esittely
Uudet koronavirukset kuuluvat 0 -sukuun. COVID-19 on akuutti hengitysvaikutus. Ihmiset ovat yleensä alttiita. Tällä hetkellä uuden koronaviruksen tartunnan saaneet potilaat ovat tärkein infektion lähde, joka perustuu nykyiseen epidemiologiseen tutkimukseen, inkubaatioaika on 1–14 päivää, enimmäkseen 3–7 päivää. Tärkeimpiä ilmenemismuotoja ovat kuume, väsymys ja kuiva yskä. Nenän ruuhkat, vuotava nenä, kurkkukipu, myalgia ja ripuli löytyy muutamassa tapauksessa.
PERIAATE
SARS-COV-2-antigeenitestille StrongStep®-järjestelmän laite käyttää immunokromatografista testiä, tämä pakkaus kerää syljenäytteitä syljen adsorptiokepistä testikortin etuosaan ja syljenäytteet etenevät kapillaarin toiminnassa. Jos näyte sisältää SARS-COV-2 N -proteiiniantigeenin. Se tunnistetaan ja sitoo lateksin pinnalla merkityt vasta-aineet immuunikompleksin muodostamiseksi. Kun muodostettu immuunikompleksi siirtyy typpihappokuidun kalvon havaitsemislinjaan pakattujen vasta-aineiden tunnistamiseksi ja fuksian havaitsemislinjan (T-LINS) muodostamiseksi, joka osoittaa SARS-COV-2-antigeenipositiivisia; Jos T-linja ei osoita väriä, se on negatiivinen tulos. Toinen linja typpihappokuitukalvossa on pakattu streptavidiinivasta -aineilla laadunvalvontalinjaksi (C -linja), jotta voidaan osoittaa tehokkaan testausprosessin.
VAROTOIMENPITEET
• Tämä pakkaus on tarkoitettu vain in vitro -diagnostiikkakäyttöön.
• Lääketieteellinen tai ei-lääketieteellinen henkilöstö voi antaa tämän pakkauksen noudattamalla käyttöohjeita.
• Lue ohjeet huolellisesti ennen testin suorittamista.
• Tämä tuote ei sisällä ihmisen lähdemateriaaleja.
• Älä käytä Kit -sisältöä päättymispäivän jälkeen.
• Käsittele kaikkia näytteitä mahdollisesti tarttuvina.
• Älä pipettireagenssia suun kautta ja tupakointia tai syömistä ei ole määrityksiä suorittaessasi.
• Käytä käsineitä koko toimenpiteen aikana.
Varastointi ja vakaus
Testisarjan suljetut pussit voidaan säilyttää 2-30 ° C: n välillä säilyvyyden ajan, kuten pussilla on osoitettu.
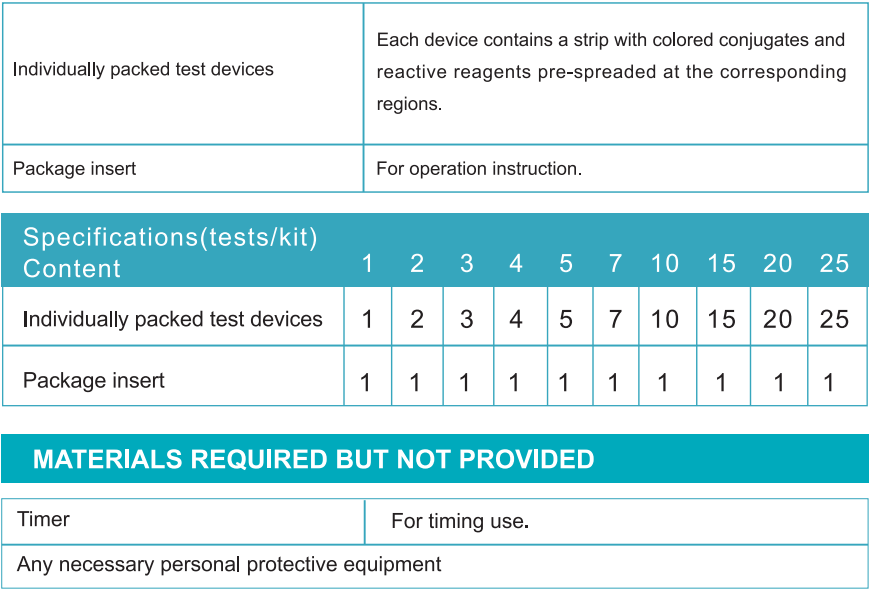
Näytteen keräys ja tallennus
Paras syljenäyte tulisi kerätä aamulla vain heräämisen jälkeen. Älä syö tai juo mitään 30 minuuttia ennen syljenäytteen keräämistä. Tee se ennen kahvia, syöminen aamiainen tai hampaiden harjaus - tai odota, kunnes et ole kuluttanut mitään edeltävänä 30 minuutissa.
Menettely
Tuo testit huoneenlämpötilaan (15-30 ° C) ennen käyttöä.
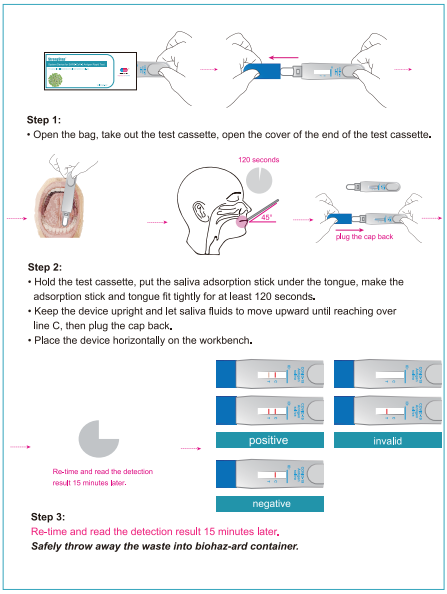
Vaihe 1:
Avaa laukku, ota testilaite pois, avaa testilaitteen pääte.
Vaihe 2:
• Pidä ketään kasettia, aseta syljen adsorptiokeppi kielen alle, tee adsorptiokeppi ja kieli sopivat tiukasti vähintään 120 sekunnin ajan.
• Pidä laite pystyssä pystyssä ja anna syljen nesteiden liikkua ylöspäin, kunnes pääset linjan C yli ja kytke sitten korkki takaisin.
• Aseta laite vaakasuoraan työpöydälle.
Vaihe 3:
Uudelleen ja lue havainto, joka resuh 15 minuuttia myöhemmin.
Heitä jätteet turvallisesti pois biohaz-ard-astiaan.
LAADUNVALVONTA
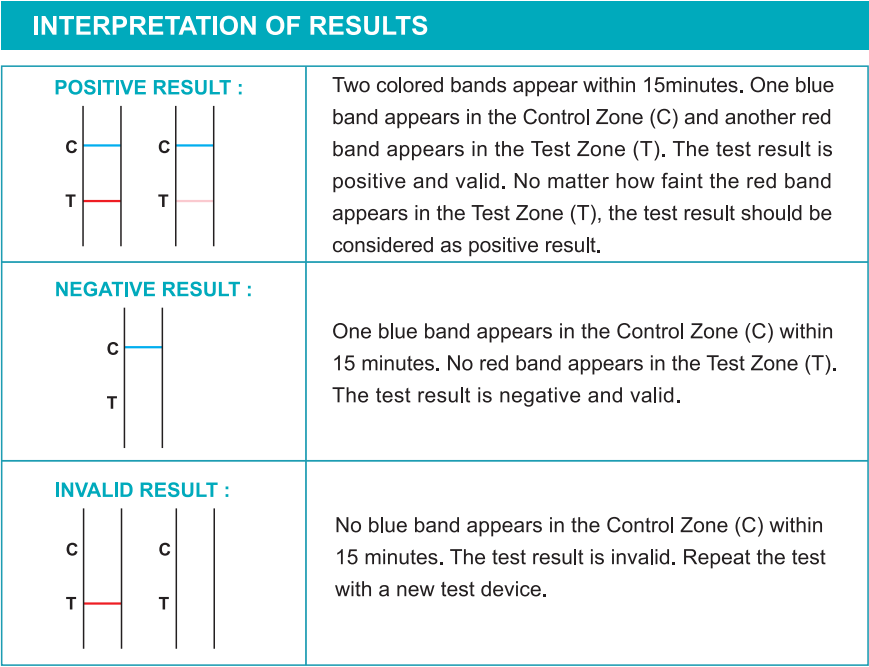
Sisäiset menettelyohjaimet sisältyvät testiin. Kontrollialueella (C) esiintyvää sinistä kaistaa pidetään sisäisenä menettelyohjauksena. Se vahvistaa riittävän näytteen tilavuuden ja oikean menettelytekniikan.
Testin rajoitukset
1. Pakkauksen tarkoituksena on käyttää SARS-COV-2-antigeenien laadullista havaitsemista syljestä.
2. Tämä testi havaitsee sekä elinkelpoisen (elävän) että ei-elinkelpoisen SARS-COV-2: n. Testisuorituskyky riippuu näytteessä olevan viruksen (antigeenin) määrästä ja voi korreloida samaan näytteeseen suoritetun virusviljelytulosten kanssa.
3. Negatiivinen testitulos voi tapahtua, jos antigeenitaso näytteessä on testin havaitsemisrajan alapuolella tai jos näyte kerätään tai kuljetetaan väärin.
4. Testimenetelmän noudattamatta jättäminen voi vaikuttaa haitallisesti testin suorituskykyyn ja/tai mitätöidä testitulos.
5. Pakkaus on tarkoitettu vain oletettuun seulontaan. Negatiiviset tulokset eivät sulje pois SARS-COV-2-infektiota ja henkilö, joka ei ole tarttuva. Jos oireita on, etsi välitöntä lisätestausta.
6. Testitulokset on korreloitava kliinisen historian, epidemiologisten tietojen ja muun lääkärin arvioinnin käytettävissä olevien tietojen kanssa.
7. Positiiviset testitulokset eivät sulje pois rinnakkaisinfektioita muiden taudinaiheuttajien kanssa, eivätkä ne välttämättä voi määrittää, onko henkilö tarttuva.
8. Negatiiviset testitulokset eivät ole tarkoitettu hallitsemaan muissa ei-SARS-virus- tai bakteeri-infektioissa.
9. Oireiden potilaiden negatiiviset tulokset tulisi käsitellä oletettuina ja vahvistettavana paikallisella FDA: lla valtuutetulla molekyylimäärityksellä tarvittaessa kliiniseen hoitoon, mukaan lukien tartunnan torjunta.
10. Näytteiden stabiilisuussuositukset perustuvat influenssatestauksen stabiilisuustietoihin ja suorituskyky voi olla erilainen SARS-COV-2: n kanssa. Käyttäjien on testattava näytteet mahdollisimman nopeasti näytteen kokoelman jälkeen.
11. alempi metodologiansa vuoksi.
12. Positiiviset ja negatiiviset ennustavat arvot ovat erittäin riippuvaisia esiintyvyysasteista.
Positiiviset testitulokset edustavat todennäköisemmin vääriä positiivisia tuloksia pienten / ei SARS-COV-2-aktiivisuuden aikana, kun taudin esiintyvyys on alhainen.FALSE-negatiiviset testitulokset ovat todennäköisempiä, kun SARS-COV-2: n aiheuttama sairauden esiintyvyys on korkea.
13. Monoklonaaliset vasta-aineet eivät voi havaita tai havaita vähemmän herkkyydellä SARS-COV-2-influenssaviruksia, joille on tehty pieniä aminohappojen muutoksia kohdeepitooppialueella.
14. Tämän testin suorituskykyä ei ole arvioitu käytettäväksi potilailla, joilla ei ole merkkejä ja hengitystieinfektioiden oireita ja suorituskykyä, voivat vaihdella oireettomilla henkilöillä.
15. Antigeenin määrä näytteessä voi vähentyä sairauden keston kasvaessa.
Sairauden 7 jälkeen kerätyt näytteet ovat todennäköisemmin negatiivisia verrattuna RT-PCR-määritykseen.
Testin herkkyyden oireiden alkamisen seitsemän päivän jälkeen on tiedetty vähentyneen verrattuna RT-PCR-määritykseen.
16. Ei ole suositeltavaa käyttää viruksen kuljetusmedia (VTM) -näytettä tässä testissä, jos asiakkaat vaativat tätä näytetyyppiä, asiakkaiden tulee vahvistaa itsensä.
17. Toistuva testaus on välttämätöntä COVID-19: n diagnoosin herkkyyden lisäämiseksi.
18. B.1.351; B.1.2; B.1.1.28; B.1.617; B.1.1.529.
19. Positiiviset tulokset osoittavat, että virusantigeenit havaittiin otetussa otoksessa, ota itsekelmikoru ja ilmoita perhelääkärille viipymättä ja/tai paikalliselle terveysosastollesi valtion vaatimusten mukaisesti.
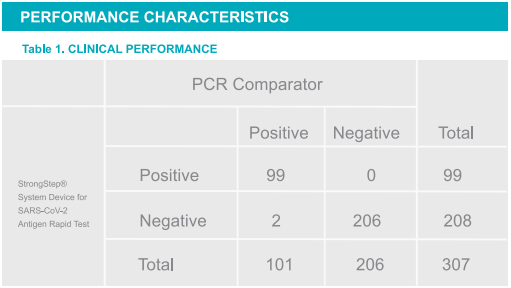
Positiivinen prosenttiosuus: (PPA) = 98,02%(93,03%~ 99,76%)*
Negatiivisen prosentin sopimus: (NPA) = 100%(98,23%~ 100%)*
Sattuen kokonaismäärä = 98,76%
*95%: n luottamusväli
Analyyttinen suorituskyky
a) havaitsemisraja (LOD):
Testin havaitsemisraja (LOD) määritettiin käyttämällä inaktivoidun SARS-COV-2: n rajoittamista. Se on SARS: ään liittyvän koronavirus-2: n (SARS-COV-2), eristävän Kiinassa CDC: ssä, joka on inaktivoinut β-propiolaktoni. Materiaali toimitettiin jäädytetty TCID -pitoisuutena505,00 x105/ml.
SARS-COV-2: n määrittämiseksi määrityksen heijastamiseksi suoraa sylkeä käytettäessä. Tässä tutkimuksessa noin 50 μl viruksen laimennusta piikkii syljen negatiivisella näytteellä.
LOD määritettiin kolmessa vaiheessa:
Kello 1. LOD -seulonta
Inaktivoidun viruksen 10-kertaiset laimennokset tehtiin negatiivisessa sylkessä ja prosessoitiin jokaiselle tutkimukselle, kuten yllä on kuvattu. Nämä laimennukset testattiin kolmena kappaleena. Kolme 3 positiivista osoitettu pitoisuus valittiin LOD -alueen löytämiseen.
2. LOD Range Finding
TCID: stä tehtiin viisi (5) kaksinkertaistumista505,00 x102/ML -pitoisuus negatiivisessa syljessä, joka on käsitelty tutkimukselle, kuten yllä on kuvattu. Nämä laimennukset testattiin kolmena kappaleena. Kolme 3 positiivista osoitettu pitoisuus valittiin LOD -vahvistukseen.
3. LOD -vahvistus
Pitoisuus tcid502,50 x102/ML -laimennus testattiin yhteensä kaksikymmentä (20) tulosta. Ainakin yhdeksäntoista (19) kaksikymmentä (20) tuloksesta oli positiivinen.
Päätelmä:
Tämän testauksen perusteella pitoisuus vahvistettiin seuraavasti:
LOD: TCID502,50 x102/ml
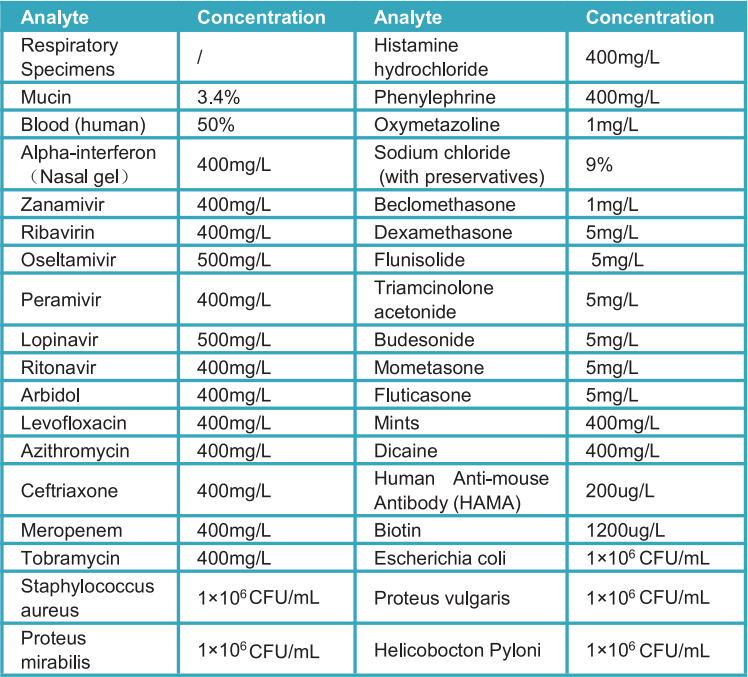
b) Ristireaktiivisuus:
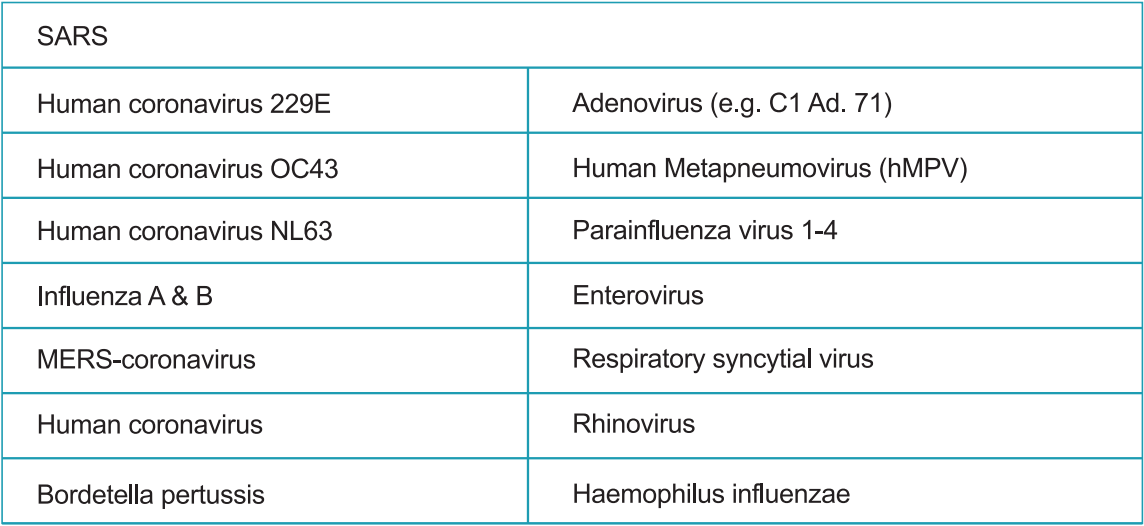
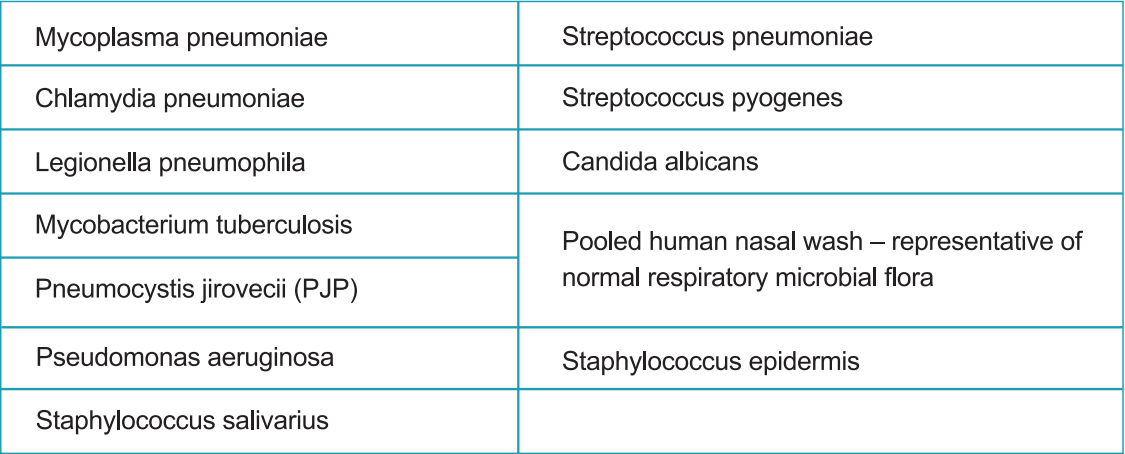
StrongStep®-järjestelmän laitteen SARS-COV-2-antigeenin nopeat testit arvioitiin testaamalla erilaisia mikro-organismeja (10⁶ CFU/ml), viruksia (10⁵ PFU/ml) ja negatiivisia matriisia, jotka saattavat mahdollisesti reagoida StrongStep®: n kanssa Järjestelmälaite SARS-COV-2 Antigeenin nopeatesti.
Jokainen organismi ja virus testattiin kolmena kappaleena. Tämän tutkimuksen tuottamien tietojen perusteella SARS-COV-2-antigeenin nopeat testit StrongStep®-järjestelmän laite ei reagoi risteykseen testattujen organismien tai virusten kanssa.
c) häiritä ainetta:
StrongStep® SARS-COV-2 -antigeenin nopeat testin mahdolliset häiritsevät aineet arvioitiin testaamalla erilaisia aineita, joiden pitoisuus oli alapuolella, mikä saattaa häiritä StrongStep® SARS-COV-2 -antigeenin nopeat testiä. Jokainen aine testattiin kolmena kappaleena. Tämän tutkimuksen tuottamien tietojen perusteella StrongStep® SARS-COV-2 -antigeenin nopeatesti ei häiritse testattuja aineita.
d) koukkuvaikutus
Korkein lämpötilan inaktivoidun SARS-CoV-2 -kannan pitoisuus (TCID505,00 x 105/ml) testattiin. Koukkuvaikutusta ei havaittu.




1人份抗原卡实物图唾液版1_00_副本-300x216.png)